您当前的位置: 新闻中心 > 企业动态
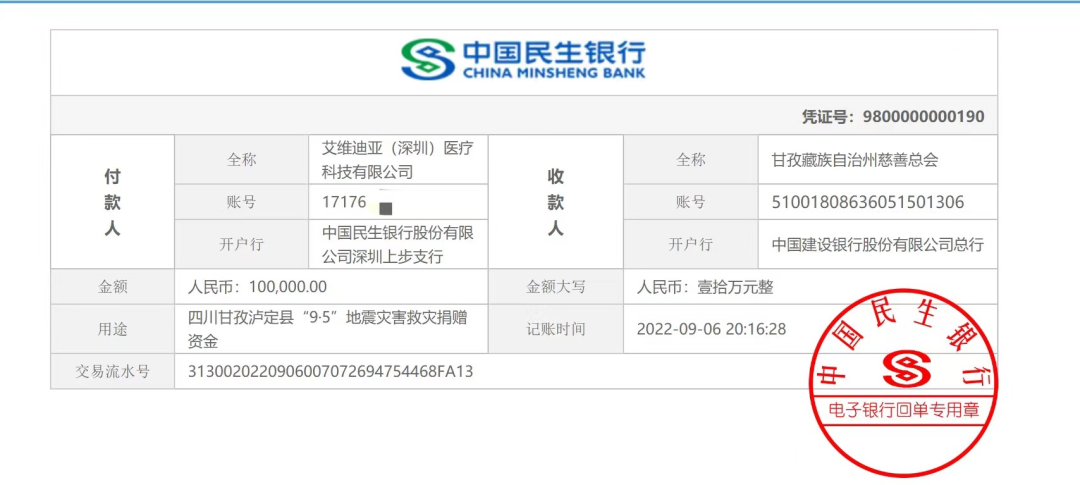
- 2022-09-06一方有难,八方支援,9月6日,IVDEAR团队通过甘孜藏族自治州慈善总会向灾区捐赠100000元人民币,支援灾后援助工作。后续,我们还将持续关注泸定地震救灾工作进展,为灾区提供力所能及的帮助,尽一份绵薄之力。愿灾区群众尽快脱离危险,早日重建美好家园!
- 2022-08-06近日,经过认证机构一系列严格的审查、考核,IVDEAR全面通过新版ISO9001国际质量管理体系认证,荣获ISO9001质量管理体系认证证书,这标志着IVDEAR已步入规范化、标准化、科学化的企业管理程序。
- 2022-08-02集合新型冠状病毒、甲型流感病毒及乙型流感病毒的抗原检测试剂盒(下称“三联检”)产品可以同时检测流感和新冠病毒,以便于在进入流感季节时可以节省检测时间和检测资源。
- 热烈庆祝SAFECARE新型冠状病毒抗原检测试剂盒(唾液)通过欧盟公告机构PCBC(公告号:1434)的认证,并正式颁发许可证。产品获证后,可在欧盟成员国以及其他认可欧盟标准的国家进行全面销售。
- 2022-08-02目前,IVDEAR团队可承接猴痘前瞻性临床实验研究项目(出具伦理批件),IVDEAR可为IVD企业提供全流程的解决方案服务。
- 2022-07-29IVDEAR可承接新冠试剂盒前瞻性临床、WHO EUL、变异病毒研究(delta、omicron BA.1、BA.2)、IVDD CE、IVDR CE、澳洲TGA、英国CTDA、欧盟HSC Common List、欧代服务、英代等全流程技术指导及服务。
- 2022-07-28美国猴痘疫情已经失控,确诊猴痘病例数3天内猛增33%,目前感染人数已达到4639例,已经超过了西班牙(西班牙报告的猴痘确诊病例为3125例),成为全球猴痘感染人数最多的国家。
- 2022-07-28近日,经过认证机构严格细致的审核,IVDEAR服务能力达到五星标准,荣获“五星级” 全国售后服务认证证书。
- 2022-07-27建议广大国内新冠企业,抓紧时间做欧盟前瞻性临床,尽早申请进入common list的A组审批列表。
- 2022-07-26IVDEAR团队可承接新冠检测试剂关于变异株BA.4、BA.5的临床实验研究项目,且可提供变异株原始测试报告,实施实验研究的临床机构具备医学实验室ISO15189资质。有需进行该实验研究的企业可与IVDEAR团队取得联络!
- 2022-07-21据世卫组织最新数据显示,目前全球70多个国家共发现近1.4万猴痘确诊病例,其中已报告的大多数猴痘确诊病例是在欧洲。确诊病例中,有5例死亡病例,均在非洲。
- 2022-08-187月15日,国家药监局器审中心发布通告,猴痘病毒核酸检测试剂国内注册即将正式启动了!